国内第Ⅱ/Ⅲ相試験(MOVER:リセドロン酸ナトリウム水和物を対照とした非劣性試験) 国内第Ⅱ/Ⅲ相試験(MOVER:リセドロン酸ナトリウム水和物を対照とした非劣性試験)
本試験におけるボンビバ静注0.5mg群は、承認外の用法および用量のため削除しています。
① 非外傷性椎体骨折(既存骨折の増悪を含む)発生頻度 [ 主要評価項目 ]
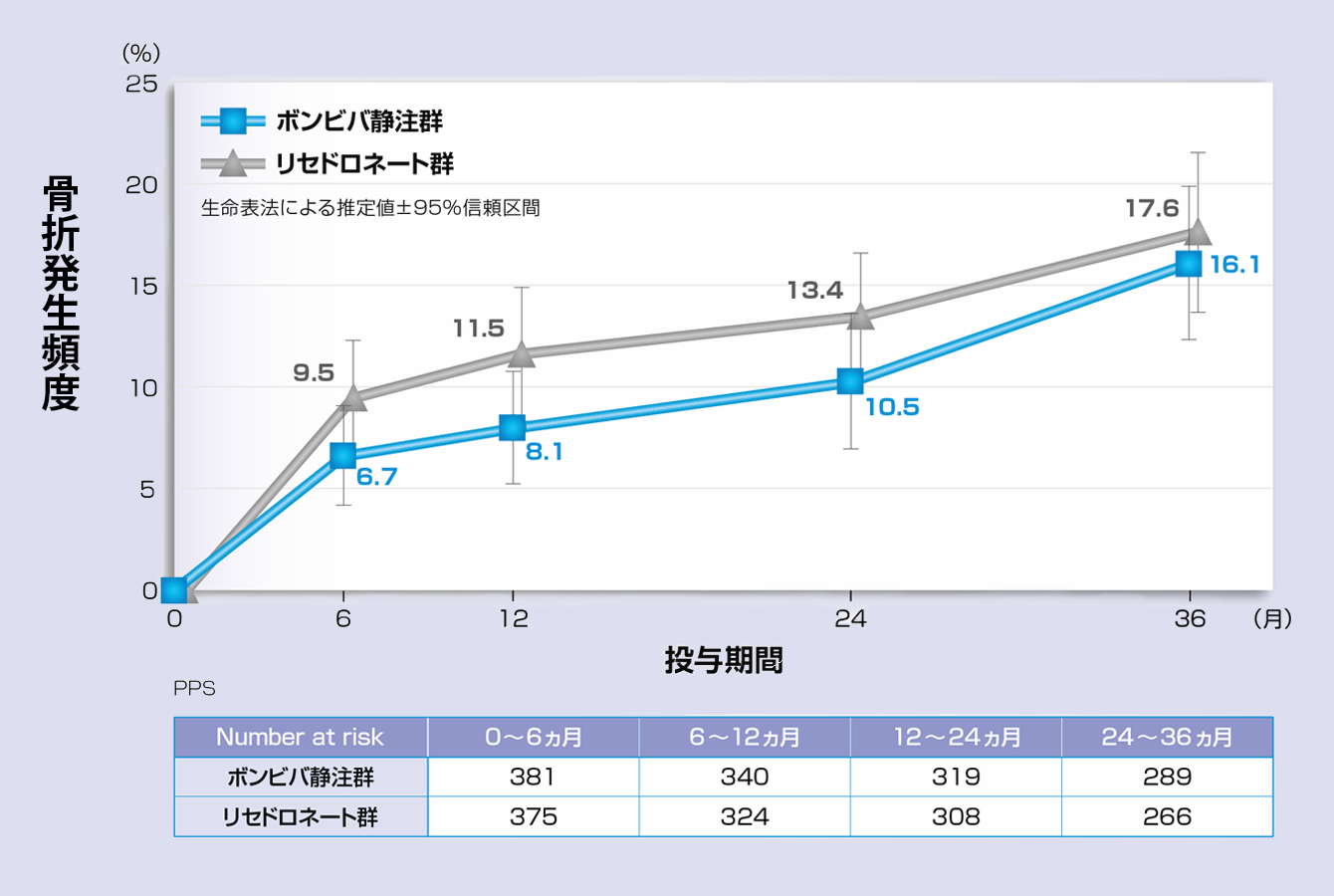
主要評価項目である非外傷性椎体骨折発生頻度について生命表法による3年間の骨折発生頻度の推定値(95%信頼区間)はボンビバ静注群16.1%(12.2~19.9%)、リセドロネート群17.6%(13.6~21.6%)でした。非外傷性椎体骨折発生頻度の層別Cox回帰分析によるリセドロネート群に対するボンビバ静注群のハザード比は0.88(90%信頼区間:0.65~1.20、95%信頼区間:0.61~1.27)であり、ボンビバ静注群のリセドロネート群に対する非劣性が検証されました(非劣性限界値1.55※1)。 非外傷性椎体骨折(既存骨折の増悪を含む)発生頻度の推定値
非外傷性椎体骨折(既存骨折の増悪を含む)発生頻度の推定値
※1:非劣性限界値の設定理由
プラセボに対するビスホスホネートのハザード比は、海外で実施されたプラセボ対照のビスホスホネートの骨折試験結果より、0.45とし、非劣性マージンはプラセボに対するビスホスホネートのハザード比の1/2(=0.611)より小さい0.55、非劣性限界値は1+0.55より、1.55とした。 国内第Ⅱ/Ⅲ相試験では、ハザード比の両側90%信頼区間の上限が非劣性の限界値(1.55)を下回れば非劣性が成り立つとした。
② 骨粗鬆症性非椎体骨折※2発生頻度 [ 副次評価項目 ]
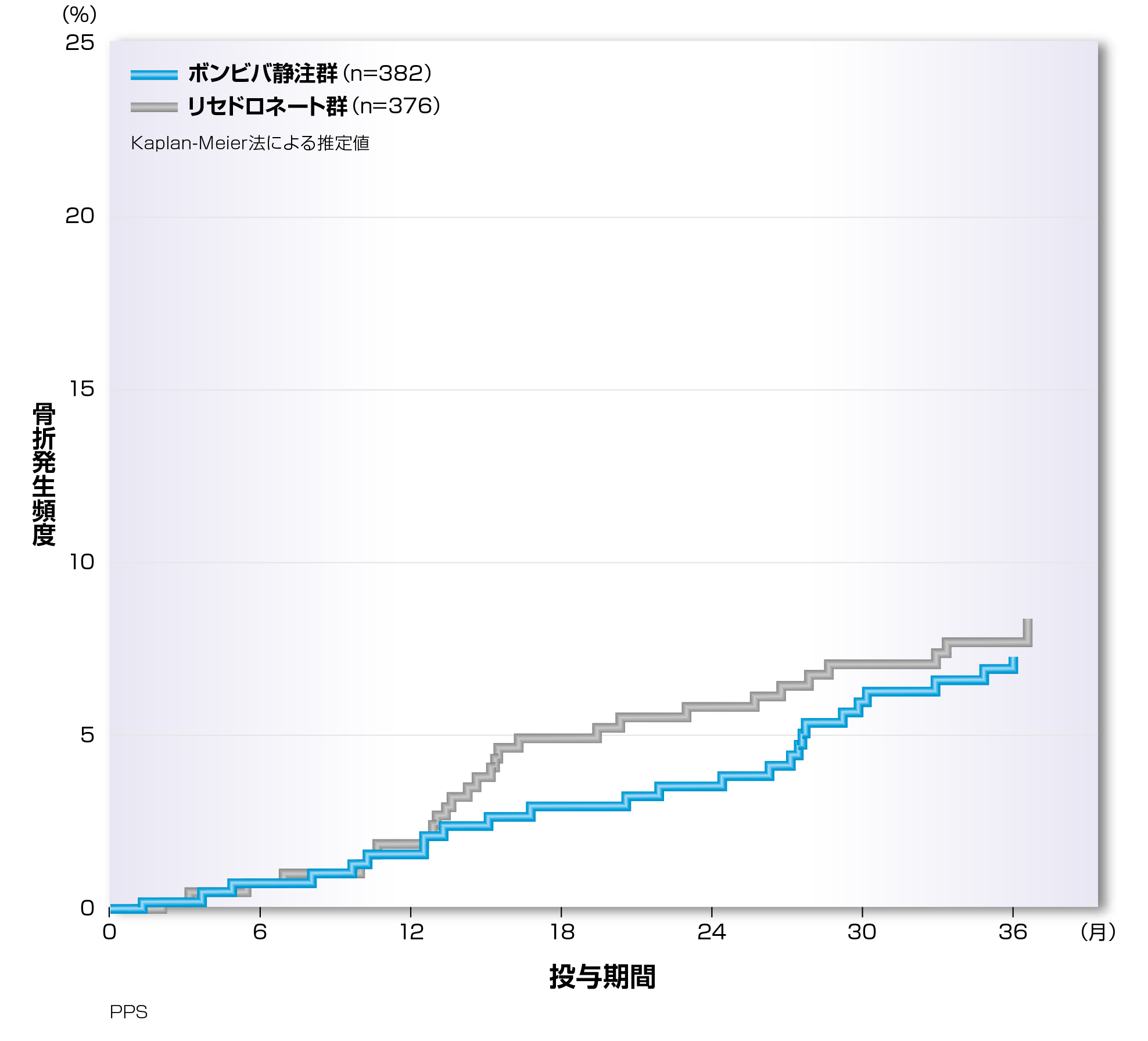
骨粗鬆症性非椎体骨折※2の経時的な発生頻度をKaplan-Meier法により推定した結果、3年間の骨折発生頻度の推定値はボンビバ静注群7.2%、リセドロネート群8.4%でした。 骨粗鬆症性非椎体骨折発生頻度の推定値
骨粗鬆症性非椎体骨折発生頻度の推定値
※2:椎体骨折および顔と手足の指等に発生した骨折を除く骨折(肋骨骨折、骨盤骨折、上腕骨骨折、前腕骨骨折、大腿骨骨折、脛骨骨折、腓骨骨折、鎖骨骨折)







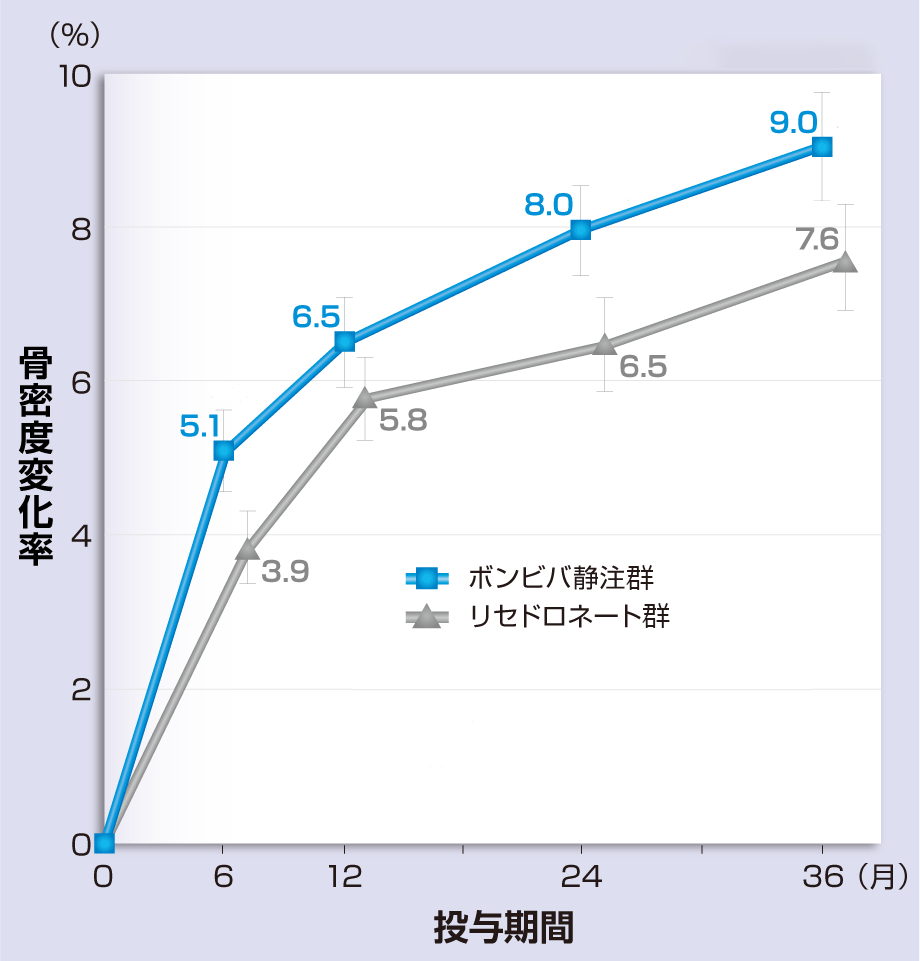

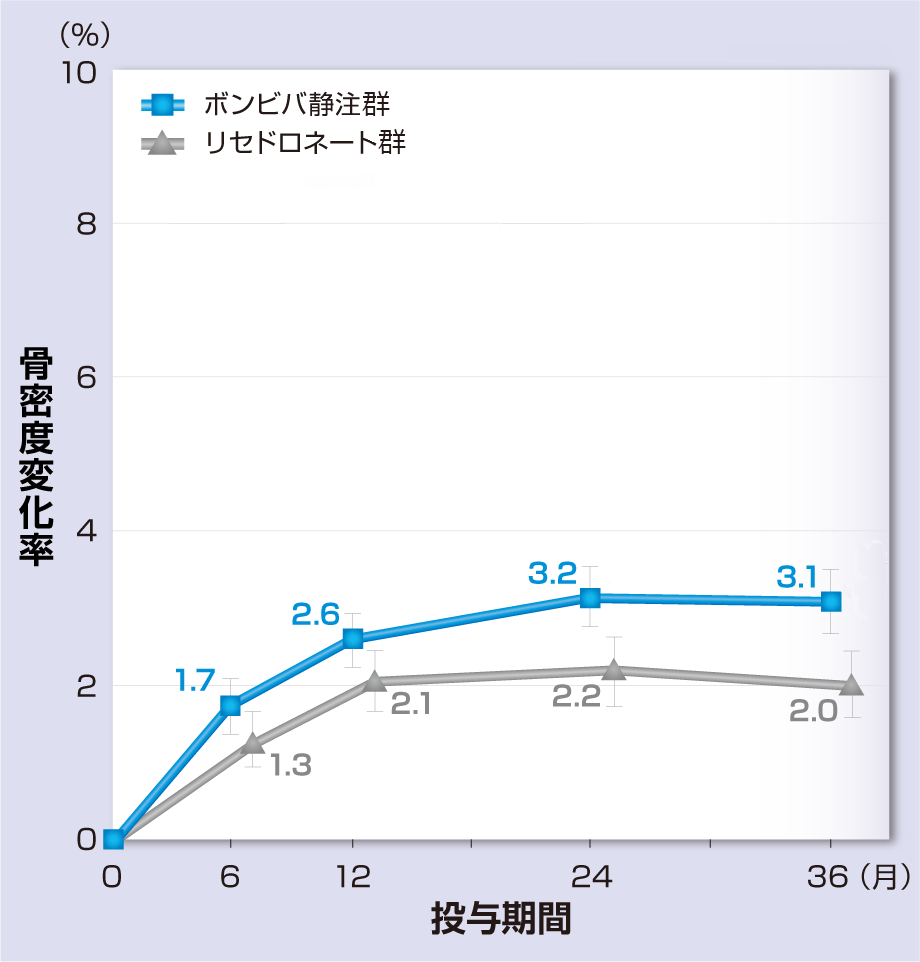

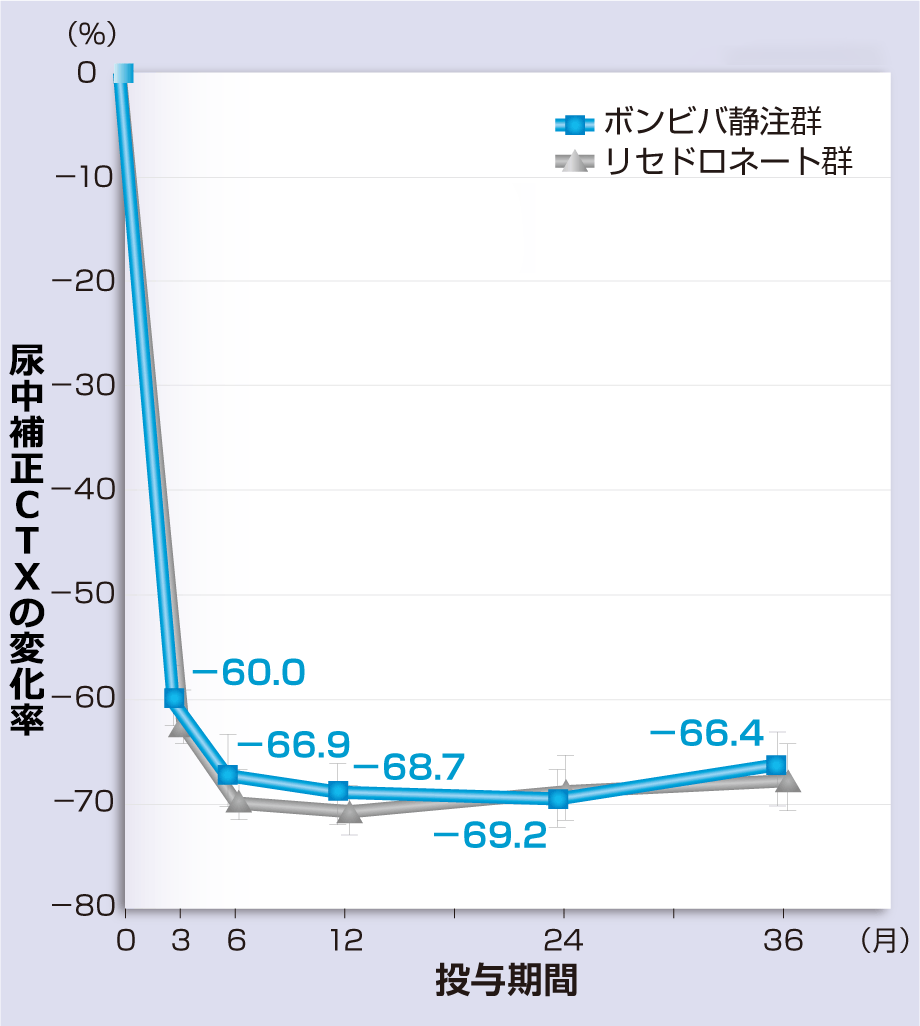

承認時評価資料[無作為化二重盲検群間比較試験(第Ⅱ/Ⅲ相試験)]
Nakamura T, et al, Calcif Tissue Int 2013; 93: 137-146.より改変
本研究は、中外製薬株式会社と大正製薬株式会社の支援によって行われた。